
Konfigurasi Elektron Pengertian Aturan Contoh Soal Dan Riset
Konfigurasi elektron adalah susunan elektron pada subkulit atom dalam orbital atom atau molekulnya. Pelajari Pengertian Aturan Gas Mulia Contoh Soal.. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6. 10 Ne = 1s 2 2s 2 2p 6.
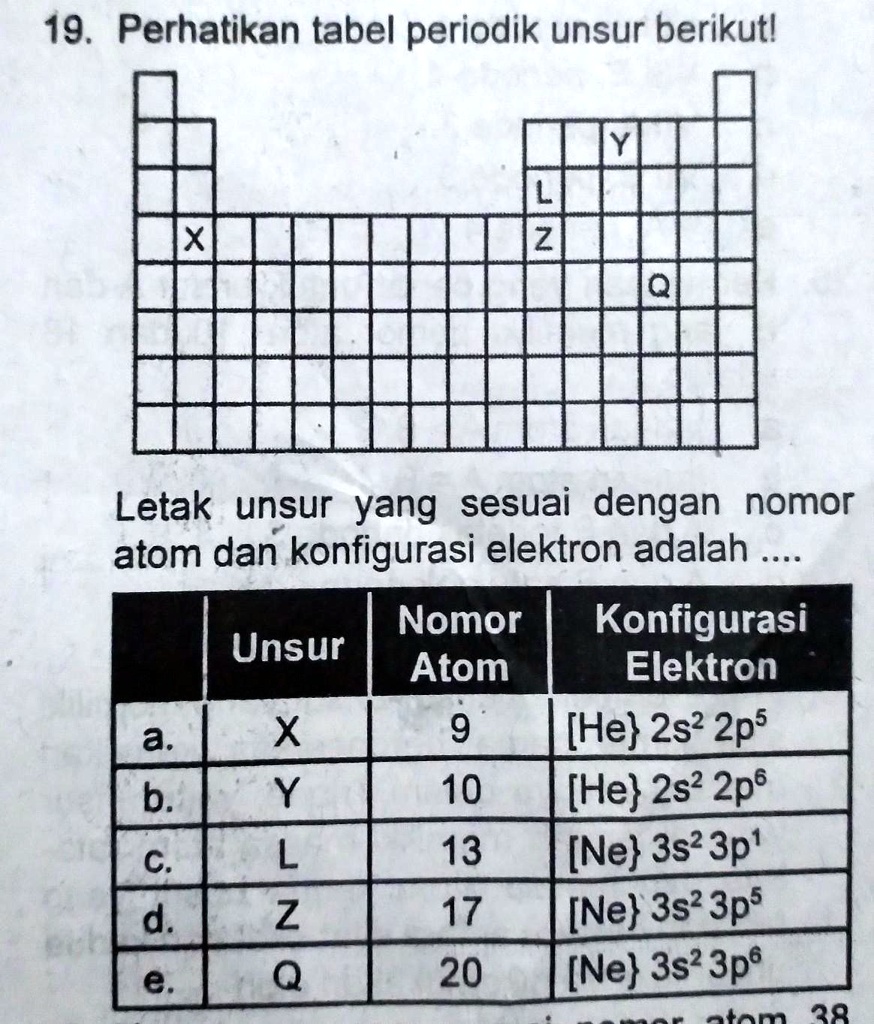
SOLVED Bantuin jawab dong hyung) 19 Perhatikan tabel periodik unsur berikutl X 2 Letak unsur
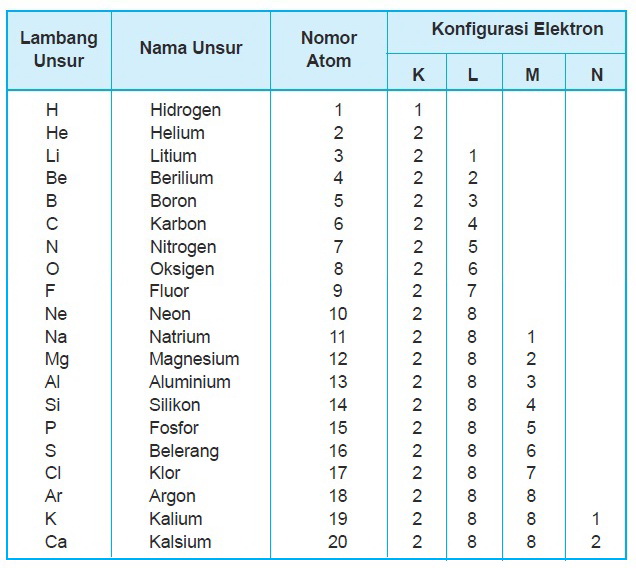
Oleh karena itu, susunan elektron valensi suatu unsur sangat mempengaruhi atau merupakan penentu sifat-sifat kimia suatu atom. Unsur-unsur yang m. Contoh Soal. Tentukan elektron valensi dari Natrium (Na)! Jawaban: Nomor atom (Z) Natrium (Na) adalah 11, maka (Na) = 2. 8. 1. Sehingga. Jumlah kulit Na = 3. Kulit terluar Na = M. Elektron valensi = 1
Teori Atom, Struktur Atom Dan Konfigurasi Elektron SMA X
Elektron valensi unsur Y adalah 3s 2 3p 5. Elektron valensi unsur Y berjumlah 7 elektron. Karena orbital terakhir adalah orbital s dan p, maka dapat disimpulkan bahwa unsur Y terletak pada golongan VIIA. Periode dapat ditentukan dengan melihat kulit (n) terbesar dalam konfigurasi elektronnya. Unsur Y memiliki kulit terbesar n = 3, sehingga.

Perhatikan konfigurasi elektron unsur dan Y berikut! Jika...
Banyaknya jumlah elektron terluar (elektron valensi) dari suatu atom menentukan sifat-sifat kimia suatu unsur. Konfigurasi elektron dapat dituliskan dengan cara: 1. Berdasarkan Kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2n2 2 n 2, di mana n menunjukkan kulit atom. Contoh: 11Na 11 N a: 2, 8, 1.

Konfigurasi elektron suatu unsur X adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d5. Unsur
Konfigurasi elektron adalah suatu susunan penyebaran (pengisian) elektron-elektron dalam . Berikut langkah konfigurasi elektron berbagai atom. Disclaimer;. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6; 10 Ne = 1s 2 2s 2 2p 6;

Cara Cepat Menuliskan Konfigurasi Elektron, Golongan, dan Periode YouTube
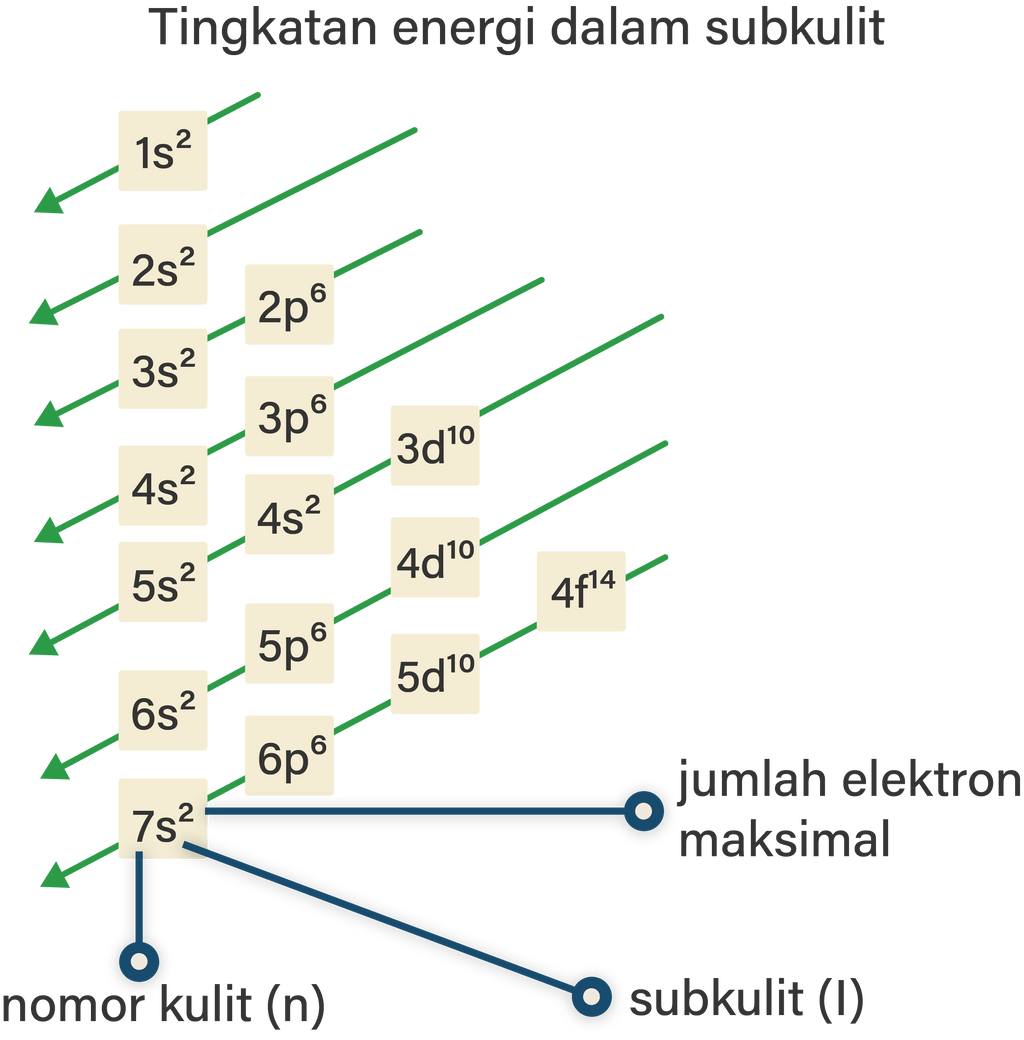
Jumlah elektron maksimal yang menempati subkulit atom adalah 2 untuk subkulit s, 6 untuk subkulit p, 10 untuk subkulit d, dan 14 untuk subkulit f. Sehingga lebih lengkapnya, konfigurasi elektron mengikuti urutan berikut. 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 14 6d 10 7p 6. Contoh: 16 S : 1s 2 2s.

Cara menulis konfigurasi elektron dan mengisi diagram orbital YouTube
Berikut ini adalah konfigurasi elektron dari unsur gas mulia: 2He = 1s2 10Ne = 1s2 2s2 2p6 18Ar = 1s2 2s2 2p6 3s2 3p6 36Kr = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 54Xe = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 86Rn = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 Konfigurasi elektron gas mulia digunakan untuk menyederhanakan.
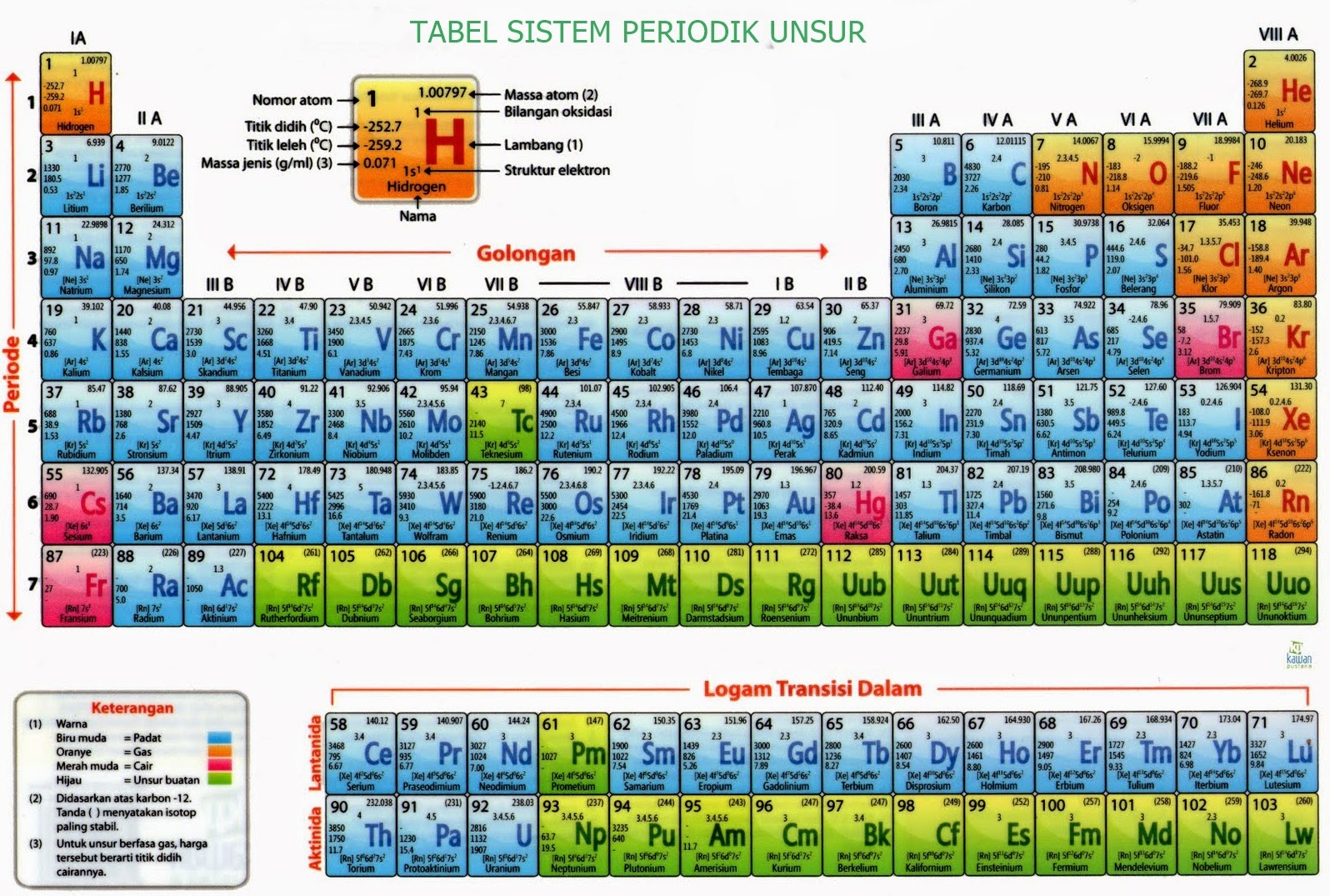
Tabel Sistem Periodik Unsur dan Penjelasannya Lengkap
Maka contoh penulisan konfigurasi elektron adalah sebagai berikut. 1s 2 2s 2 2p 6 3s 2 3p 4. Pengecualian; Terdapat beberapa aturan pengecualian untuk pengisian konfigurasi elektron. Seperti yang pertama yaitu dalam aturan Aufbau kita diharuskan mengisi elektron dalam orbital sesuai dengan urutan tingkat energinya.
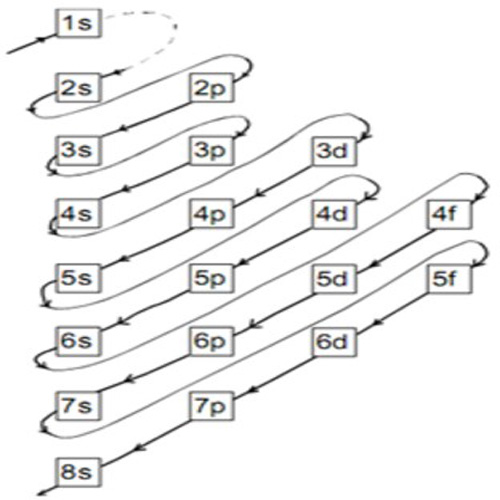
Pengertian Konfigurasi Elektron Rumus Kimia
Contoh soal 9. Konfigurasi elektron empat unsur adalah: P = 1s 2 2s 2 2p 6 3s 2 3p 6. Q = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3p 8. R = 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 3. S = 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2. Pernyataan yang benar tentang unsur-unsur tersebut.. A. unsur P terletak dalam golongan 8.

Cara Menentukan Konfigurasi Elektron
Konfigurasi elektron adalah susunan elektron dalam tingkat energi di sekitar inti atom. Menurut teori atom, keberadaan elektron menempati beberapa tingkat dari kulit pertama yang terdekat dengan inti atom, yaitu kulit K, hingga kulit ketujuh Q, yang memiliki letak paling jauh dari inti atom.. Bila kita perhatikan diagram orbital unsur S pada.

Pengertian Konfigurasi Elektron Ilmu Kimia
Konfigurasi elektron gas mulia digunakan untuk menyederhanakan atau meringkas konfigurasi elektron unsur yang lain. Misalnya konfigurasi elektron atom Mn adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d5, jika disederhanakan dapat ditulis 25Mn [Ar] 4s2 3d5 atau 25Mn [Ar] 3d5 4s2. Baca juga:
Jelaskan tentang konfigurasi elektron beserta cont...
Berdasarkan urutan nomor atom pada tabel periodik di atas, nomor atom unsur Q adalah 20. Maka, konfigurasi elektron aufbau unsur Q : Jadi, jawaban yang tepat adalah B. Konfigurasi elektron merupakan susunan elektron pada lintasan kulitnya. Pengisian konfigurasi elektron aufbau disusun secara urutan berdasarkan tingkat energi subkulit dari yang.
Konfigurasi Elektron Pengertian, Cara Menentukan, & Contoh Soal
Konfigurasi elektron. Konfigurasi elektron atom gas netral dalam keadaan dasar. Disajikan berdasarkan subkulit dalam bentuk ringkas, dengan subkulit ditulis, dan dengan jumlah elektron per kulit. Konfigurasi elektron setelah unsur nobelium (unsur 102) adalah tentatif dan setelah rutherfordium (unsur 104) adalah prediksi.
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
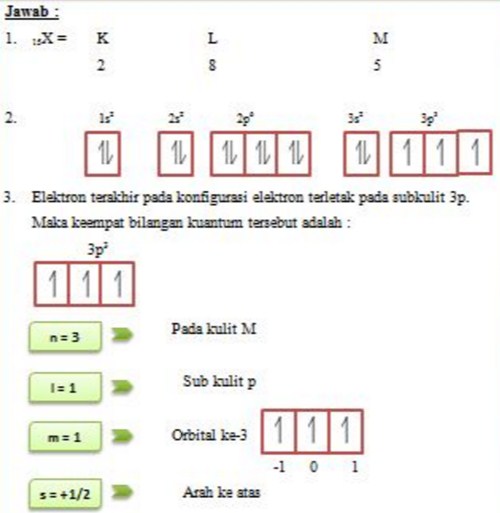
Aturan Penulisan Konfigurasi Elektron. Berdasarkan teori atom Niels Bohr, elektron pada atom akan menempati kulit-kulit atom. Kulit K adalah kulit yang paling dekat dengan inti atom biasa ditempati oleh 2 elektron. Sementara pada kulit kedua yakni kulit L akan ditempati oleh 8 elektron, terus berikutnya hingga kulit paling luar dari atom.

Konfigurasi elektron suatu unsur adalah 1s^2 2s^2 2p^6 3s...
Sisa elektron adalah 24, dimana 18 < 24 < 32, sehingga untuk kulit keempat kita isikan 18 elektron. 52 Te : 2 8 18 18. Sampai di sini, jumlah elektron yang tersisa adalah 6. Sesuai dengan aturan pertama, sisa elektron ini langsung kita isikan pada kulit terakhir. Jadi, konfigurasi elektron dari atom Telurium adalah. 52 Te : 2 8 18 18 6

Konfigurasi Elektron Pengertian Notasi Dan Tabel Periodik
Dalam teori ini, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) paling rendah, yaitu kulit yang pertama kulit K, setelah kulit K sudah terisi penuh, dilanjutkan ke kulit L, kulit M, kulit N, hingga seterusnya. Jumlah elektron maksimal yang ditempati setiap kulit elektron, dapat diketahui menggunakan rumus : 2.n2