Kelemahan Model Atom Rutherford Teori Dan Model Atom Muatan Negatif My XXX Hot Girl
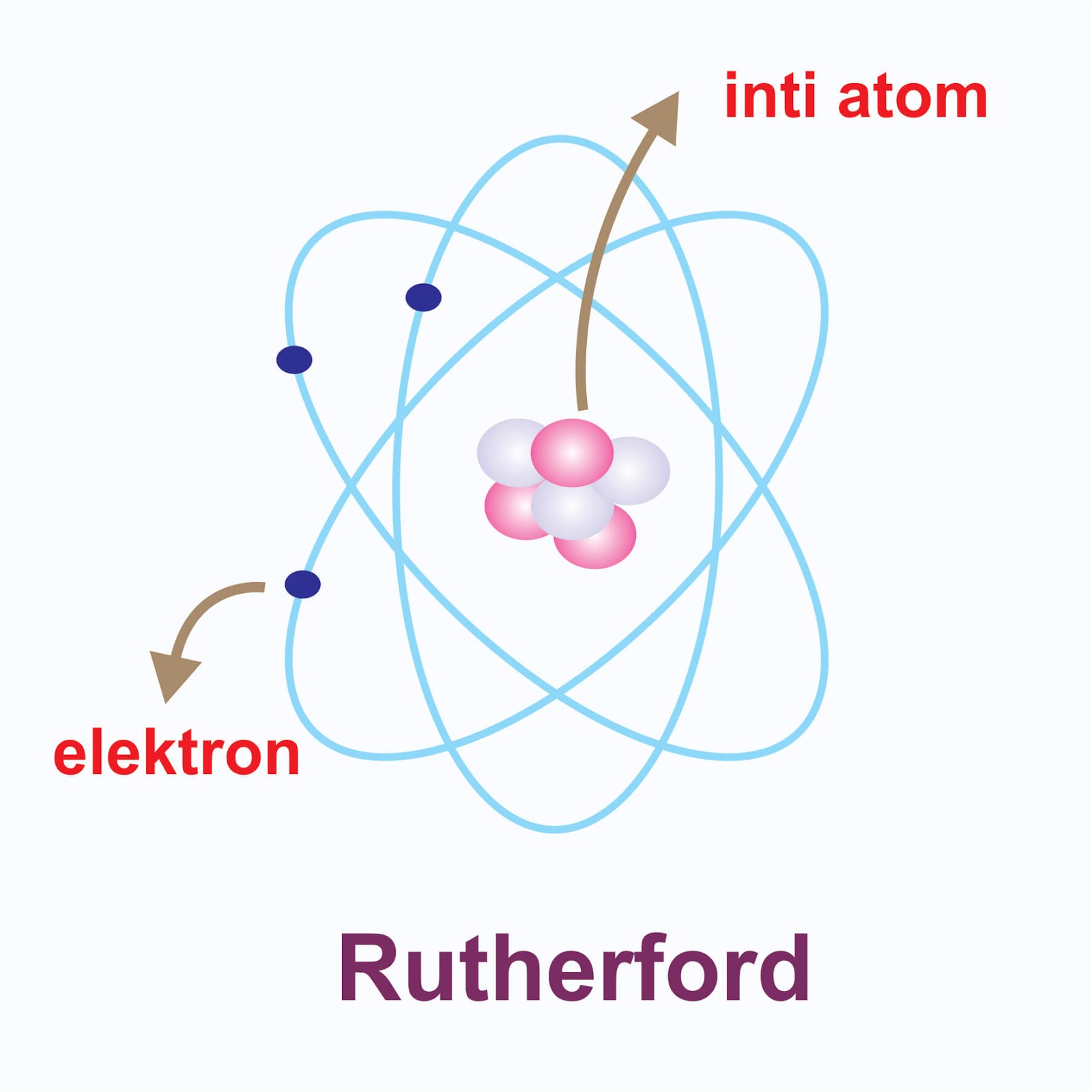
Setelah elektron ditemukan oleh J. J. Thomson, ilmuwan berikutnya yang mengemukakan teori model atom adalah Ernest Rutherford. Rutherford melakukan eksperime.

Kelemahan Teori Atom Rutherford Adalah Tidak Adanya Penjelasan Tentang
MagicBricks.com is India's No 1 Property portal and has been adjudged as the most preferred property site in India, by independent surveys. The portal provides a platform for property buyers and sellers to locate properties of interest and source information on the real estate space in a transparent and unambiguous manner.

Teori dan model atom Rutherford I Eksperimen I Kelebihan & Kelemahan Teori Atom Rutherford YouTube
Hal ini menjadi salah satu kelemahan yang dimiliki teori atom Rutherford. Untuk membuat suatu kajian teori yang langsung sempurna, teori atom Rutherford terus dikembangkan dan disempurnakan oleh para ilmuwan lainnya. Elektron yang mengelilingi inti atom, akan mengalami kehabisan tenaga dan bisa membuat proses perputaran menjadi terhambat. 2.

Perkembangan Teori Atom Dan Model Atom Seputar Model
Baca juga: Perkembangan Teori Atom: Model Dalton, Thomson, Rutherford, dan Bohr. Sehingga, kelemahan Teori Atom Niels Bohr adalah hanya mampu menjelaskan spektrum atom sederhana seperti hidrogen dan tidak dapat menjelaskan atom-atom yang lebih kompleks. Tidak bisa menjelaskan Efek Zeeman. Kelemahan lain teori atom Bohr adalah tidak dapat.
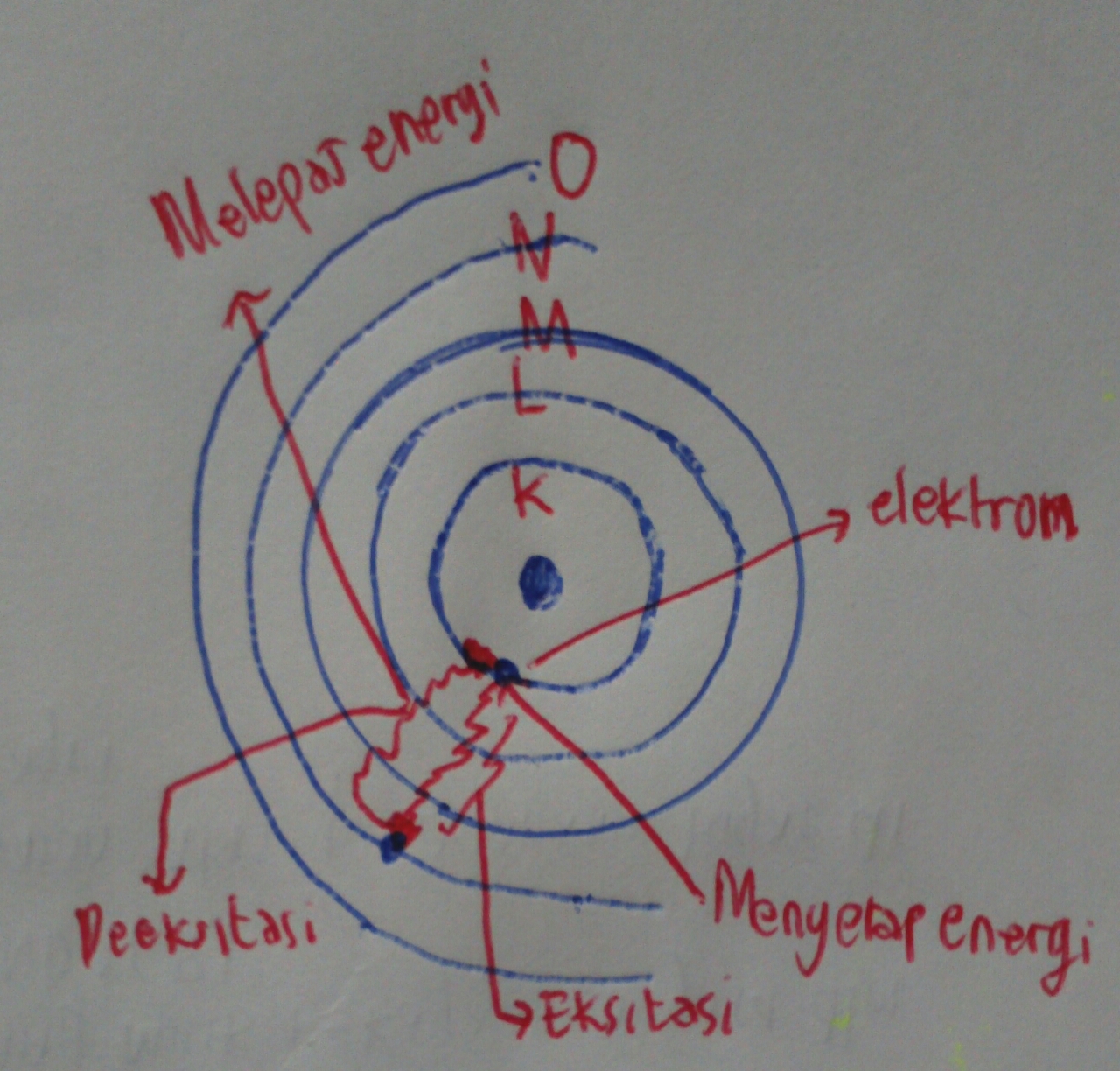
Kelemahan Dan Kelebihan Teori Atom Rutherford
Teori Rutherford sendiri berkembang mulai tahun 1911. Isi dari teori atom ini sebenarnya untuk menyangkal teori model atom milik J.J Thomson. Atom Rutherford mendapatkan teorinya berdasarkan percobaan Geiger-Marsden yang terjadi pada tahun 1909. Ia melakukan percobaan dan menunjukkan adanya kekeliruan dalam teori yang Thompson kemukakan.
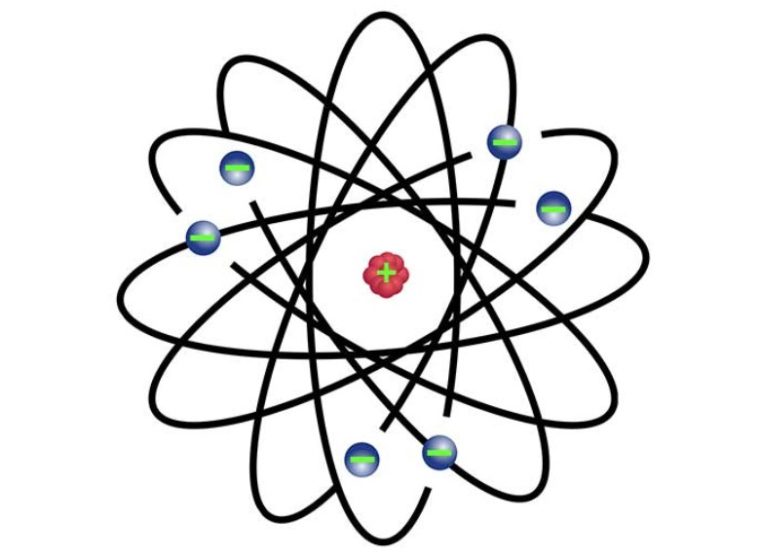
Kelebihan Dan Kelemahan Atom Rutherford
Penjelasan Niels Bohr dalam menjawab kelemahan teori atom Rutherford menjadi salah satu kontribusi besar dalam fisika modern. Pada tahun 1911 Ernest Rutherford mengajukan teorinya bahwa atom itu terdiri dari inti yang sangat padat berisi muatan positif disertai partikel-partikel kecil yang bergerak dengan kecepatan tinggi di sekelilingnya.

Kelebihan Dan Kelemahan Atom Rutherford
Teori atom modern terdiri dari 5 model, yaitu model atom Dalton, Thomson, Rutherford, Bohr dan mekanika kuantum. Atom menurut Dalton adalah partikel terkecil dari suatu materi berbentuk seperti bola pejal yang tidak dapat dibagi lagi serta tidak dapat diciptakan dan dimusnahkan. Suatu atom terdiri dari sebuah inti (di pusat atom) yang sangat.

Kelebihan dan Kekurangan Teori Atom Rutherford
Namun, teori ini memiliki kelemahan yaitu tidak mampu menjelaskan penyebab elektron tidak jatuh ke inti atom selama elektron mengelilingi inti atom. 4. Teori atom Niels Bohs Niels Bohr memperbaiki model atom Rutherford. Niels Bohr, adalah seorang ilmuwan fisika yang berasal dari Denmark. Ia mengembangkan teori struktur atom pada 1913.

TEORI MODEL ATOM RUTHERFORD! KELEBIHAN & KELEMAHAN Teori Atom Pt.3 Kimia X YouTube
Sehingga, teori atom Rutherford yang telah dikemukakan ini lebih mudah untuk dimengerti dan dipahami khususnya dalam menggambarkan struktur atom yang kelihatan rumit sekali. Kelemahan Teori Rutherford. Selain kelebihan yang terdapat dalam teori atom Rutherford, tentu terdapat beberapa kelemahan dalam teori atom Rutherford yang telah dikembangkan.

Kelemahan Teori Atom Rutherford
Kelemahan dan Limitasi Teori Atom Rutherford. Meskipun memiliki kelebihan yang signifikan, dan juga didasarkan pada pengamatan eksperimental, namun terdapat kelemahan dan keterbatasan yang perlu diakui, yaitu: 1. Tidak Menjelaskan Stabilitas Atom.

Kelemahan Teori Atom Rutherford Kelemahan Teori Atom Rutherford Berikut beberapa inti atau
Teori atom Rutherford menjelaskan tentang atom memiliki inti yang bermuatan positif dan dikelilingi oleh elektron yang mengelilinginya. Kelemahan teori atom Rutherford adalahtidak dapat menjelaskan alasan elektron tidak jatuh ke inti.Elektron-elektron yang mengelilingi inti secara terus menerus akhirnya akan kehilangan energi dan kemungkinan dapat menumbuk inti atom.
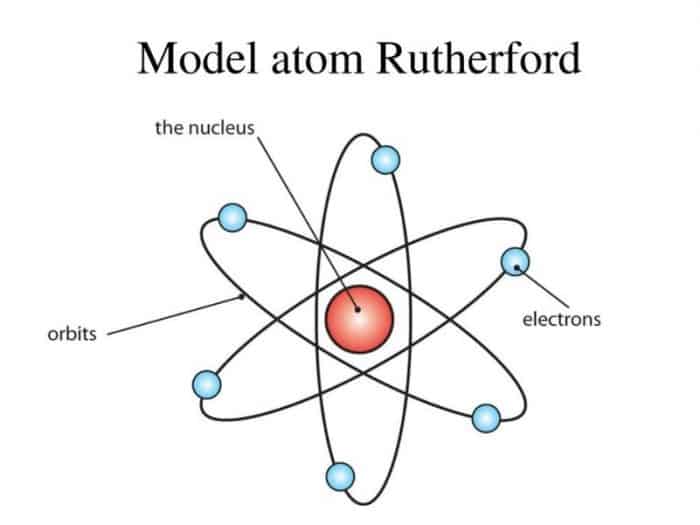
Teori Struktur Atom Menurut Para Ahli Beserta Pengertiannya (Lengkap)
Kelebihan dan Kelemahan Atom Rutherford. Meskipun penemuan ini menjadi titik cerah dalam pemahaman struktur atom, teori ini memiliki sejumlah kekurangan dan kelebihan. Dikutip dari buku Praktis Belajar Kimia, Iman Rahayu (2007:29), berikut uraiannya. 1. Kelebihan Atom Rutherford. 2. Kekurangan Atom Rutherford.

Kelebihan Dan Kelemahan Atom Rutherford
Sebenarnya percobaan tersebut dilakukan oleh Rutherford untuk membantah hasil ilmuwan sebelumnya, yakni J.J Thomson. Dari hasil uji kimia sebelumnya dikatakan bahwa apakah atom sebagai bola pejal positif apabila dikenai partikel alpha akan dipantulkan. Teori atom yang dikemukakan Rutherford ini memiliki rumusan model, kelebihan, serta.

Perbedaan teori atom dalton, thomson, rutherford, niels bohr
Perkembangan Teori Atom: Model Dalton, Thomson, Rutherford, dan Bohr. KOMPAS.com - Konsep atom sebagai partikel terkecil di alam semesta, dicetuskan oleh Demokritos di masa Yunani Kuno. Namun karena teori itu tak disertai penelitian ilmiah, banyak ilmuwan yang meragukan dan meneliti kebenarannya. Baru pada abad ke-19, atom diteliti secara.

Kelemahan Teori Atom Rutherford Adalah Tidak Adanya Penjelasan Tentang
Setelah melakukan beberapa percobaan, Rutherford mengusulkan suatu model atom yang dikenal dengan model atom Rutherford. Isi teori atom Rutherford, antara lain: Namun, teori atom Rutherford ini memiliki beberapa kelemahan. Berikut ini kelemahan-kelemahan teori atom Rutherford, dikutip dari buku Praktis Belajar Kimia untuk Kelas X Sekolah.

Kelebihan Dan Kekurangan Atom Rutherford Brain
Kelebihan teori atom Rutherford. Menemukan atom merupakan inti (terdiri dari proton dan neutron) yang dikelilingi oleh elektron yang bermuatan negatif. Menemukan bahwa inti atom sangat kecil namun berkontribusi sebagai hampir keseluruhan massa atom. Menemukan bahwa elektron sangat ringan namun berkontribusi sebagai hampir keseluruhan volume atom.