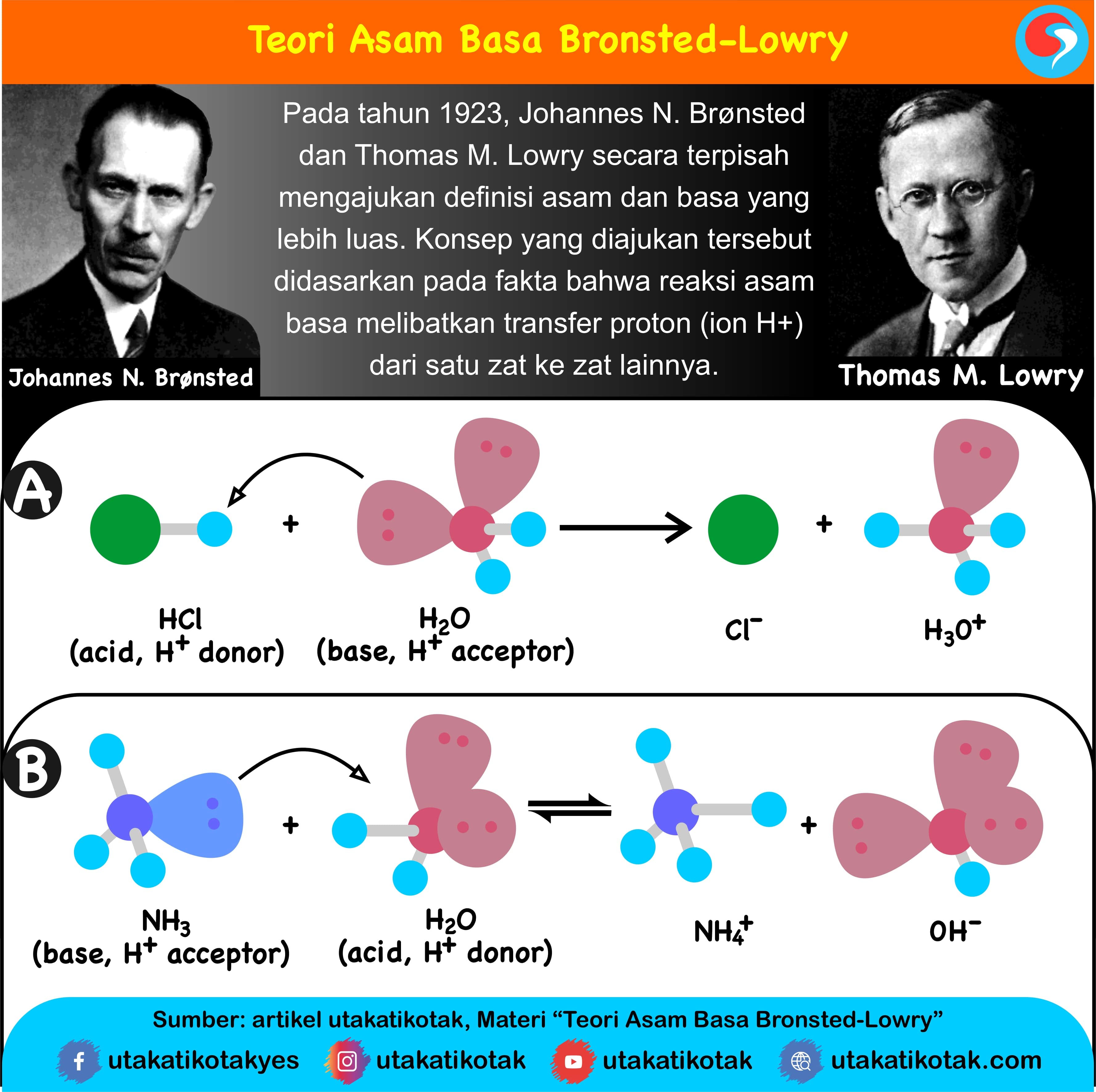
Teori Asam dan Basa Menurut BronstedLowry
Di artikel Kimia kelas 11 ini, kita akan belajar mengenai macam-macam indikator asam basa dan cara menggunakannya. Yuk, baca sampai habis! Teman-teman, di artikel sebelumnya, kamu sudah mengenal apa itu zat asam-basa dan cara membedakannya, ya. Senyawa asam akan mengandung ion H +. Contohnya buah-buahan kaya vitamin C, cuka, minuman bersoda, dsb.

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
1. Ciri-ciri Asam • Asam kuat tidak dianjurkan untuk dikonsumsi karena mampu merusak kulit. • Asam kuat juga mampu merusak kayu. • Dapat menyebabkan karatan saat terkena logam atau besi. • Dapat menghantarkan listrik karena memiliki kandungan elektrolit. 2. Ciri-ciri Basa • Mempunyai rasa pahit • Basa murni berbentuk seperti kristal padat

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Asam asetat adalah sejenis asam lemah. Ketika larutan asam asetat dilarutkan dalam air, sebagian molekulnya akan terionisasi menjadi ion hidrogen (H+) dan ion asetat (CH3COO-). Namun, sebagian besar molekul asam asetat tetap utuh dan tidak terionisasi.

Teori Asam Basa
Kalau pada suhu 25℃, pH < 7 bersifat asam, pH = 7 bersifat netral, dan pH > 7 bersifat basa. Derajat keasaman dan kebasaan suatu larutan. (dok. Flickr/boellstiftung) Semakin kecil nilainya, maka larutan tersebut akan semakin asam. Misalnya antara larutan dengan pH 3 dan 1, akan lebih kuat konsentrasi asam dengan pH 1 daripada 3.

Hcooh Termasuk Asam Atau Basa
sehingga didapatkan rumus perhitungan konsentrasi titrasi asam basa sebagai berikut: V 1 x K 1 = V 2 x K 2 K 2 = (V 1 x K 1 V 2 Dimana: V 1 = volume analit atau zat yang dititrasi; K 1 = konsentrasi zat yang dititrasi; V 2 = volume titran terpakai; K 2 = konsentrasi titran. Jika zat asam atau basa dalam titrasi memiliki valensi lebih dari 1.
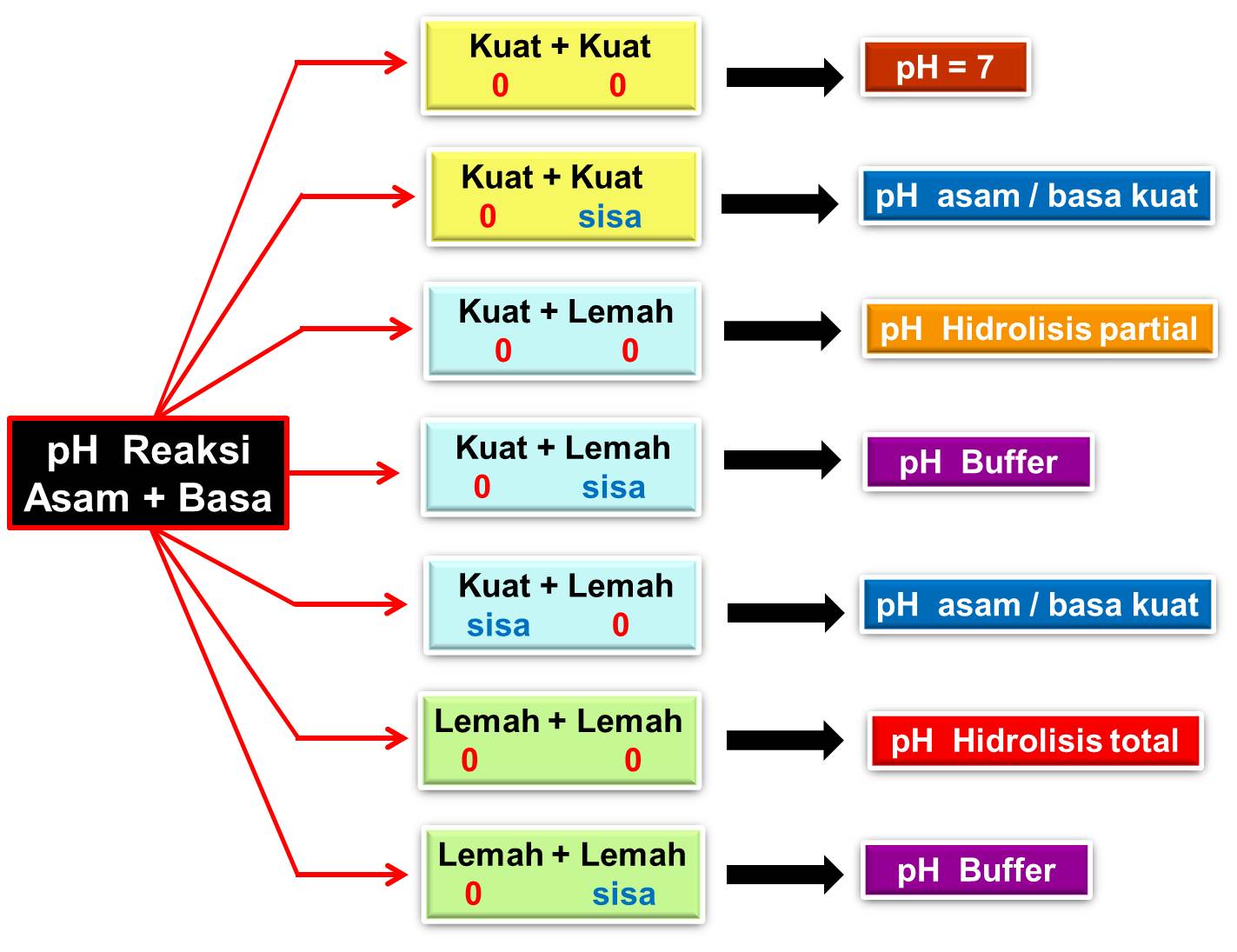
CINTA KIMIA PETA KONSEP pH REAKSI ASAM BASA
Basa kuat adalah hidroksida-hidroksida logam alkali dan alkali tanah yang larut (Ca2+, Sr2+, and Ba2+). Zat-zat ini juga terdisosiasi sempurna dalam larutan air memberikan ion hidroksi (OH-). Berdasarkan definisi merupakan elektrolit kuat dan berada sempurna sebagai ion-ion dalam larutan air. Untuk basa kuat → [OH-] = [basa].
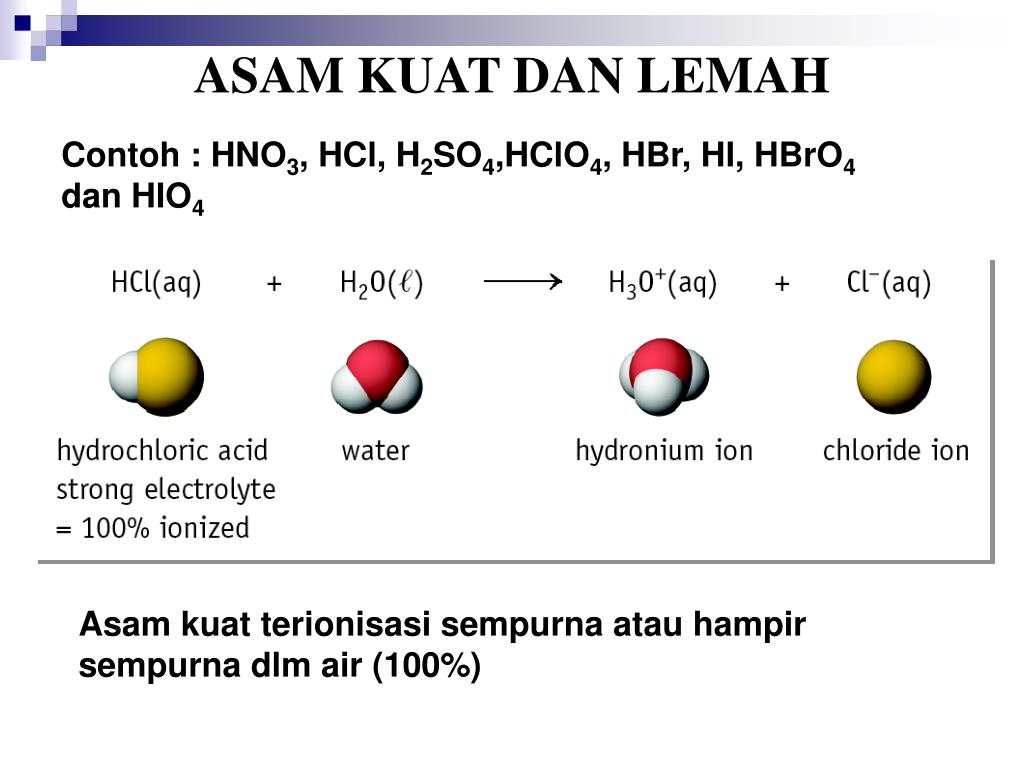
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Proses titrasi asam basa melibatkan larutan asam kuat atau basa kuat yang bisa berbahaya bagi tubuh, jadi harus dilakukan di dalam laboratorium dengan didampingi oleh guru atau asisten laboratorium. Sebelum melakukan eksperimen ini pun, kamu harus mengenakan alat pelindung diri seperti baju atau jas lab, sarung tangan, dan kacamata ( goggles.

Uji Asam Basa Menggunakan Indikator Alami Praktikum Kimia Kelas 11 MIPA YouTube
Dalam ilmu kimia saat ini, asam diartikan sebagai senyawa yang jika dilarutkan dalam air maka pH nya < 7 atau lebih kecil dari 7. Hal itu memang benar karena sifat-sifat yang dimiliki oleh senyawa asam antara lain adalah: 1. Rasanya pada umumnya masam karena mengandung asam sitrat (pada buah-buahan) 2. Sebagian besar larut dalam air 3.
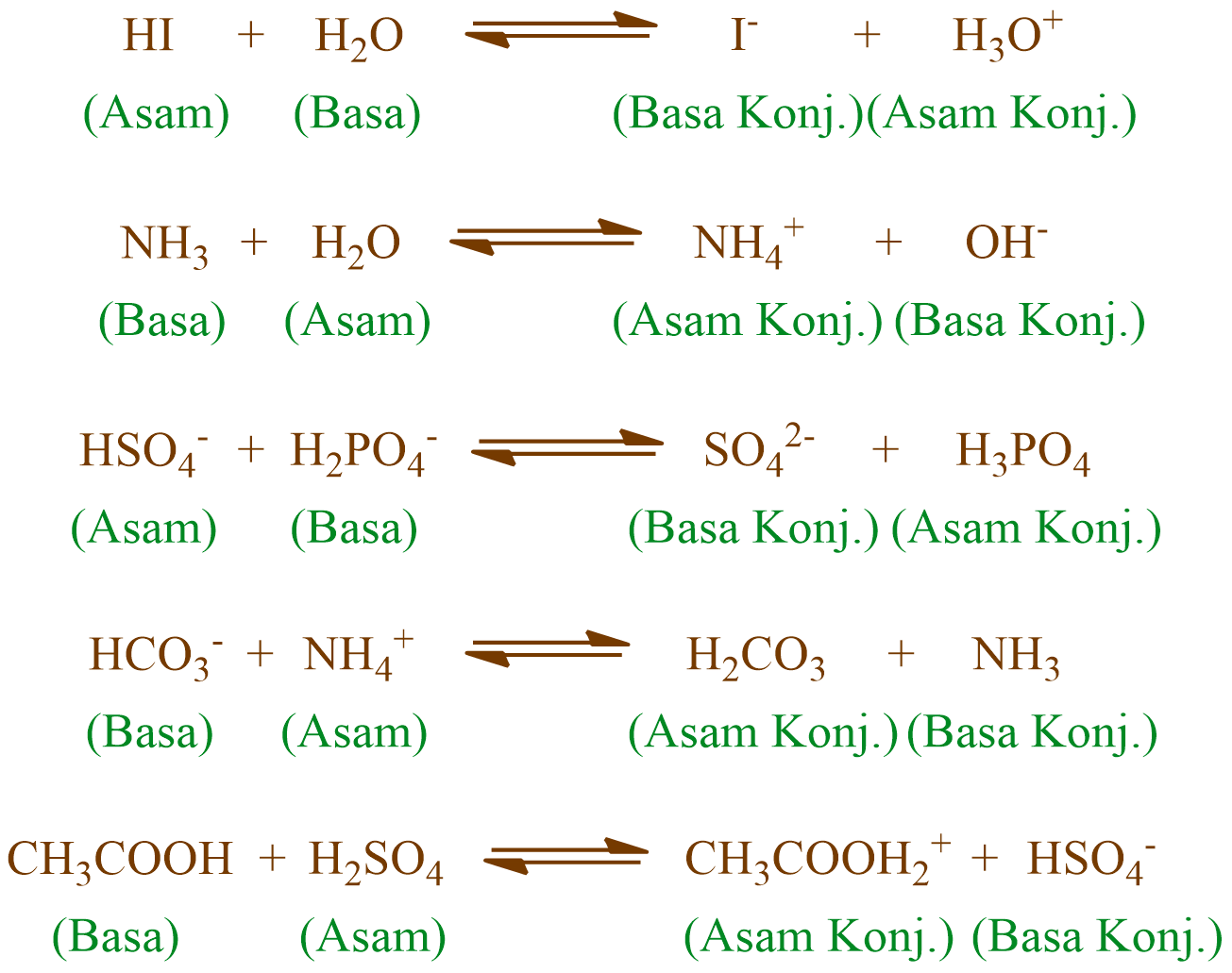
Chocogreentea Keterbatasan Teori AsamBasa Bronsted Lowry
Svante August Arrhenius, seorang ahli kimia asal Swedia yang hidup tahun 1859-1927 menjabarkan pengertian asam sebagai: semua zat atau senyawa elektrolit yang jika dilarutkan dalam air akan terurai menghasilkan ion H+ (hidrogen) dan ion sisa asam yang bermuatan negatif, demikian menurut Modul Guru Pembelajar IPA Terapan SMK.
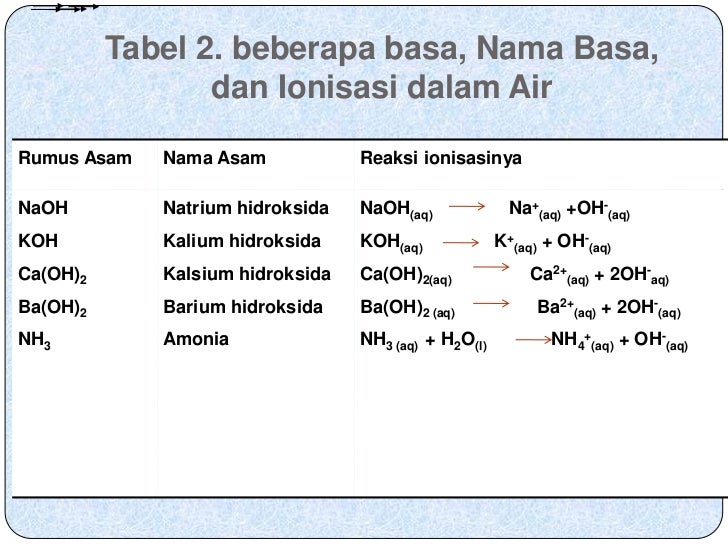
Contoh Asam Basa Kuat Dan Lemah Serta Reaksi Ionisasinya Berbagai Contoh
Contoh soal asam basa ini telah kami lengkapi dengan kunci jawabannya. Selain itu, kamu juga bisa mendownload contoh soal asam basa ini lohh.. Sebanyak 5 mL larutan HCOOH (Ka =4 x 10^-4) dengan pH 4 ditambah air sehingga pH nya menjadi 5. Volume larutan menjadi . . . .mL. A. 100. B. 250. C. 495. D. 500. E. 1000. Jawaban: D. Soal No. 14.
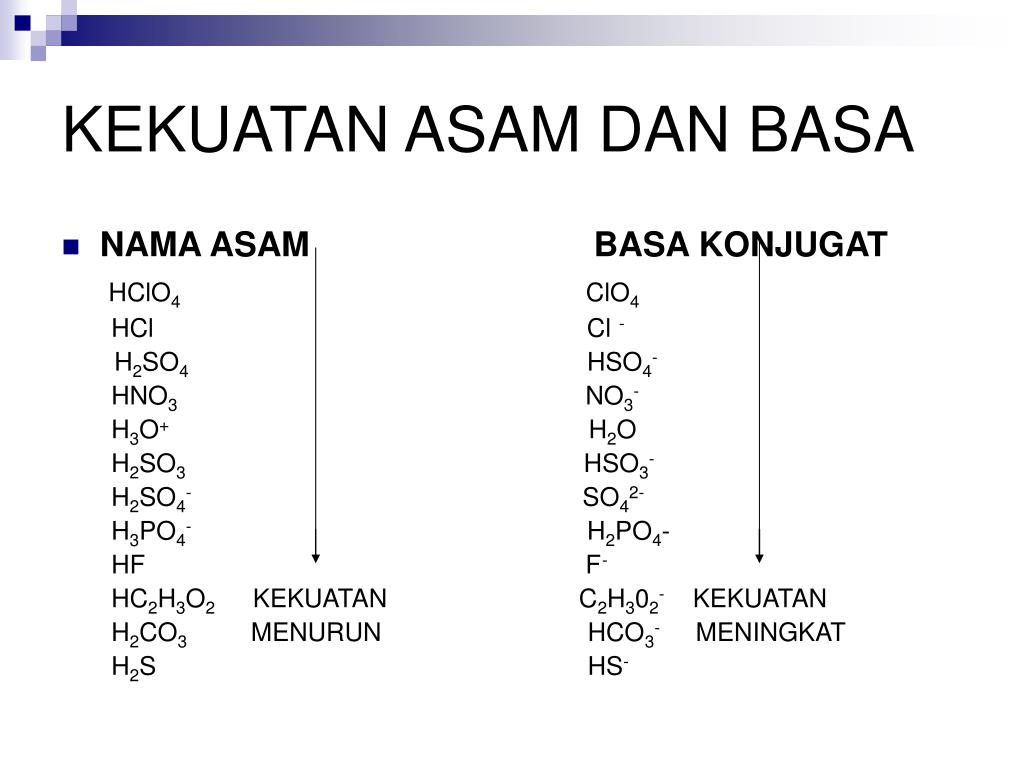
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Asam bromida (HBr) Asam sulfat (H2SO4) Asam klorat (HClO3) Sementara itu, basa kuat merupakan senyawa basa yang dapat dengan mudah melepaskan ion OH- di dalam air dan dalam larutannya terjadi disosiasi total. Misalnya seperti: Barium hidroksida (Ba (OH2) Stronsium hidroksida (CsOH) Kalsium hidroksida (Ca (OH2) Litium hidroksida (LiOH)
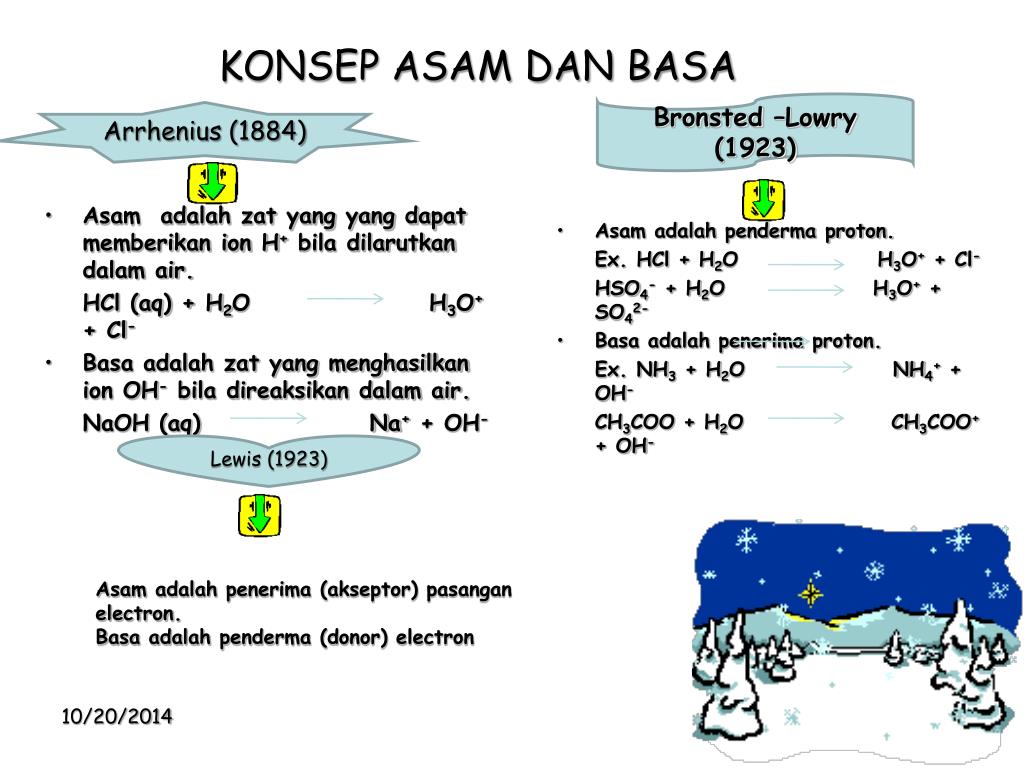
PPT ASAM BASA PowerPoint Presentation, free download ID5640840
asam lemah (contoh: HF, HCN, HNO 2, CH 3 COOH, H 2 CO 3) Dalam air, hanya sebagian asam lemah terurai menjadi ion-ionnya, sehingga derajat ionisasinya 0 < α < 1. Jika konsentrasi awal larutan asam lemah HA dinyatakan sebagai M a, maka: HA (aq) ⇌ H + (aq) + A − (aq) Mula-mula : M a Reaksi : −αM a + αM a + αM a Setimbang : (1 − α)M a αM a αM a

Pengertian Asam dan Basa Serta Penggunaannya
Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20. H20 bersifat basa karena ia menerima donor H+.
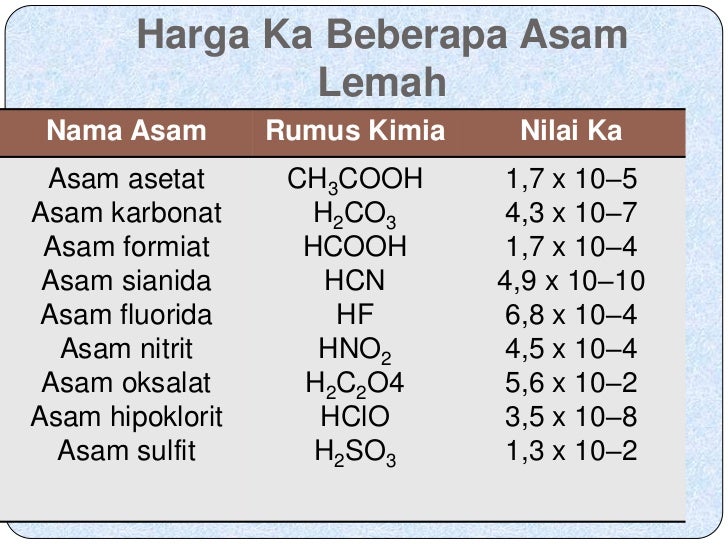
Nama Asam Dan Basa Beserta Rumus Kimianya
Apa yang dimaksud dengan larutan asam basa? Kita mulai dari larutan asam dahulu yuk, Sobat. Larutan asam adalah larutan yang memiliki pH kurang dari 7. Eh, apa pula pH itu? pH adalah ukuran yang digunakan untuk menentukan tingkat keasaman atau kebasaan suatu larutan. Sifat asam dan basa suatu larutan ditentukan oleh kandungannya.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Berikut adalah daftar nama asam kuat: Asam klorida (HCl) Asam nitrat (HNO3) Asam sulfat (H2SO4) Asam klorat (HClO3) Asam perklorat (HClO4) Asam bromida (HBr) Asam hidrogen iodida (HI) Baca juga: Hujan Asam: Penyebab, Proses, Dampak, dan Cara Mencegahnya Asam lemah Asam lemah adalah larutan dengan pH di bawah tujuh dan di atas tiga.

PPT TEORI ASAM DAN BASA PowerPoint Presentation, free download ID3560268
Asam dan basa adalah larutan elektrolit yang dikenal dengan ciri khasnya, seperti asam yang memiliki rasa masam dan basa yang memiliki rasa pahit. Asam dan basa pengertian menurut Kamus Besar Bahasa Indonesia (KBBI), asam adalah zat yang dapat memberikan proton, zat yang dapat membentuk ikatan kovalen dengan menerima sepasang elektron.